ПЛАЗМОЛИФТИНГ КАК ИННОВАЦИОННЫЙ МЕТОД ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ ПАРОДОНТА НА ЭТАПЕ ПОСЛЕВУЗОВСКОГО ОБУЧЕНИЯ
«МЕЖДУНАРОДНЫЙ ЖУРНАЛ ЭКСПЕРИМЕНТАЛЬНОГО ОБРАЗОВАНИЯ», Издательство: Издательский Дом "Академия Естествознания" (Пенза), ISSN: 19963947, № 41, 2014 г, стр. 253255.
Таранова Н. Ю., Виниченко Е.Л., Перова Н.Ю., Борискова И.В. ГБОУ ВПО КубГМУ Минздрава России, ГБОУ «Краснодарский краевой базовый медицинский колледж» Министерства здравоохранения Краснодарского края, Краснодар, Россия.
Воспалительные заболевания пародонта являются не только общемедицинской, но и социальной проблемой, так как распространенность и интенсивность хронического пародонтита довольно высокая. Несмотря на наличие большого числа предложенных методик (использование остеопластических материалов, методик направленной регенерации тканей и др.), проблема лечения пародонтита остается актуальной. Поэтому широкое внедрение новых технологий в стоматологическую практику необходимо для улучшения качества оказания помощи пациентам с заболеванием пародонта [3, 4]. Особенностью современного стоматологического образования является приоритет практической направленности выпускников медицинских вузов. Занимаясь последипломным образованием интернов, ординаторов, курсантов на кафедре стоматологии ФПК и ППС КубГМУ, преподаватели кафедры создают все условия для проведения практической части учебного процесса на высоком уровне. Врачи интерны и курсанты участвуют в научно исследовательской деятельности кафедры и в практическом изучении современных медицинских технологий, освоение которых позволяют будущему и реально функционирующему специалисту выполнять профессиональные задачи на высоком уровне мастерства. В частности, методику плазмолифтинга мы рекомендуем к использованию в повседневной практике врача-стоматолога [2, 4, 5]. Известным фактом является несоответствие сроков заживления костных тканей и слизистой оболочки. Иногда после качественно проведенной операции в области межзубных сосочков происходит заживление вторичным натяжением, что вызывает вымывание остеопластического материала и врастание в пародонтальный карман эпителия, а, следовательно, отсутствие в дальнейшем регенерации и угнетение репаративных процессов в тканях пародонта [6]. В свою очередь, быстро заживающие раны мягких тканей должны осуществлять барьерную функцию, то есть предотвращать вторичное инфицирование и агрессивное воздействие слюны на костную рану [7, 8]. В настоящее время проводятся активные исследования, посвященные изучению способов повышения эффективности существующих костных материалов и мембран. Перспективным методом в решении данной задачи является плазмолифтинг, разработанный Р.Р. Ахмеровым и Р.Ф. Зарудий – это инъекционное введение в ткани организма богатой тромбоцитами плазмы (P.R.P.), полученной из крови самого пациента [1, 2]. Аутогенные факторы роста (мы использовали F.R.P. – тромбоциты, богатые фибрином) применяли инъекционно непосредственно в области хирургического вмешательства и по переходной складке в постоперационном периоде. Целью настоящей работы явилась оценка эффективности плазмолифтинга при лечении генерализованных пародонтитов средней и тяжелой степени. Работа выполнена на базе хирургического отделения (хирургического кабинета) стоматологической поликлиники Кубанского государственного медицинского университета в период 20122013 гг. Метод плазмолифтинга использовался в комбинации с традиционным хирургическим лечением соответствующей патологии. Всего оперировано 89 пациентов с генерализованным пародонтитом (табл.). После проведения лоскутных операций в пародонтальные карманы укладывали остеопластический материал. Операционная рана покрывалась мембраной для направленной регенерации тканей, затем накладывались швы на рану. F.R.P. получали из венозной крови пациента в безвибрационной центрифуге «EBA 20» фирмы Hettich Zentrifugen с заранее отрегулированным режимом работы (6000 оборотов в минуту, в течение 10 минут). Из пробирки исполь зовалась жидкая фракция крови, которая вводилась инъекционно по переходной складке верхней и нижней челюстей. В одно посещение вводилось 34 мл плазмы не сколькими инъекциями на равном расстоянии друг от друга (по 0,3мл в каждой инъекции). Курс проводился в три-пять посещений с интервалом 56 дней.
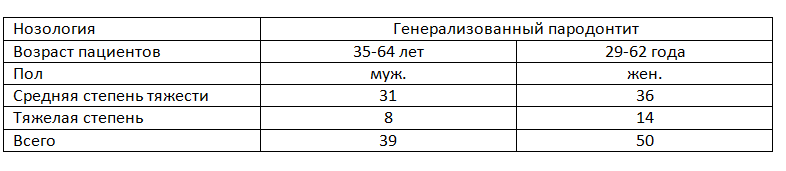
Таблица. Количество оперированных пациентов по возрасту, полу и степени тяжести.
На следующие сутки после хирургического вмешательства у большинства пациентов полностью отсутствует болевой синдром и отмечается незначительный коллатеральный отек в области вмешательства. Во всех случаях проведенного вмешательства заживление операционной раны происходило первичным натяжением. Швы снимали на 89 сутки. Всем пациентам помимо оценки динамики раневого процесса проводилось рентгенологическое обследование (ортопантомограмма) до и через три месяца после оперативного лечения, по которым оценивали динамику костной регенерации. Оценка панорамных снимков показала, что использование F.R.P. при выполнении хирургических вмешательств на пародонте позволяет стимулировать минерализацию костной ткани в области нанесения остео пластического материала. Данный эффект объясняется местной доставкой факторов роста. Таким образом, применение метода плазмолифтинга с получением F.R.P. позволяет ускорить заживление костных и мягких тканей при проведении пародонто логических хирургических вмешательств. Предварительная оценка результатов использования F.R.P. позволила нам сделать следующие принципиальные заключения: 1. Использование мембран из аутокрови практически не имеет противопоказаний. 2. В послеоперационном периоде отмечается значительное снижение болевого синдрома и выраженности воспалительных изменений мягких тканей. 3. Сроки заживления операционных ран мягких тканей сокращаются примерно в 1,5 раза. 4. Значительно улучшаются процессы минерализации и созревания кости, повышается эффективность использования остеопластических материалов. Таким образом, использованный метод плазмолифтинга с получением F.R.P. непосредственно перед операцией исключает риск развития аллергических, иммуногенных реакций и переноса инфекционных заболеваний; позволяет повысить эффективность и сократить сроки лечения пациентов. Полученные положительные результаты исследования мы включили в программу обучения врачей-стоматологов на факультете повышения квалификации в качестве инновационного метода лечения распространенных воспалительных заболеваний пародонта. Данный метод является перспективным направлением в хирургической стоматологии и требует дальнейшего развития и углубленного научного исследования.
Литература:
1. Ахмеров Р.Р., Зарудий Р.Ф., Рычкова И.Н., Исаева М.Г., Алтыева А.Ф. «Аутостимуляция регенеративных процессов в челюстнолицевой хирургии и косметологии» Методическое пособие. – Москва. 2011. 55с.
2. Зорина О.И., Грудянов А.И., Бяко ва С.Ф. Хирургическое лечение заболеваний пародонта с использованием материалов для направленной тканевой регенерации//Терра Медиа.2003.№2.с.21.
3. Махмутова А.Ф. Эффективность комплексного восстановительного лечения больных с воспалительными заболевания ми пародонта: Автореф.дис.канд.мед.наук. Москва. 2009.23с.
4. Разрешение на применение новой медицинской технологии от 26.10.2010 ФС №2010/380 «Аутостимуляция регенеративных процессов при лечении пародонтита и атрофических состояний мягких тканей средней зоны лица».
5. Howell T., Fioellini J., Paquette D. et al. A phase I/TI clinical trial to evaluate a combination of recombinant human plateletderived growth factorBB and recombinant human insulinlike growth factorI in patients with periodontal disease. // J. Periodontаl. 1997.Vol. 68(1).Р.186193.
6. Marx R., Carlson E., Eichstaedt R. et al. Plateletrich plasma. Growth factor enhancement for bone grafts.// Oral Surg. Oral Med. Oral Pathol. Oral Radial. Ended 1998. P.638646.
7. Marx R., Garg A. Bone Graft Physiology with Use of PlateletRich Plasma and Hyperbaric Oxygen. In: The Sinus Bone Graft. Jensen O, ed. Chicago: Quintessence publishing. 1998. P. 183189.
8. Tanabe SI., C. Bodet, D. Grenier Treponema denticola peptidoglycan induces the production of inflammatory mediators and matrix metalloproteinase in macrophagelike cells //J. Periodontal. 2009.Vol. 44(4). P. 503510.